Cómo prevenir la sensibilidad dental: causas y soluciones para una sonrisa sin molestias
Factores como el desgaste del esmalte o la retracción gingival pueden provocar hipersensibilidad, pero existen tratamientos y hábitos clave para controlarla, según especialistas

La sensibilidad dental afecta a 1 de cada 3 adultos en algún momento de su vida, según datos de la Federación Dental Internacional (FDI). Este molesto dolor transitorio, que aparece al consumir alimentos fríos, calientes o ácidos, no solo impacta en la calidad de vida, sino que puede ser señal de problemas bucales subyacentes que requieren atención profesional.
¿Por qué ocurre la sensibilidad dental?
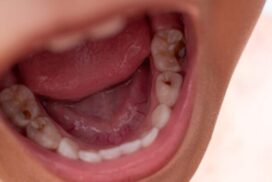
La hipersensibilidad surge cuando la dentina (capa interna del diente) queda expuesta debido a:
Retracción de encías (por cepillado agresivo o enfermedad periodontal).
Erosión del esmalte (por ácidos de alimentos, bebidas o reflujo gástrico).
Bruxismo (el rechinamiento desgasta las superficies dentales).
Tratamientos dentales recientes (como blanqueamientos o limpiezas profundas).
Tipos de pastas y tratamientos para dientes sensibles
Los dentífricos desensibilizantes son la primera línea de defensa. Su eficacia radica en ingredientes activos como:
Nitrato de potasio: bloquea las señales nerviosas.
Arginina + carbonato de calcio: sella los túbulos dentinarios.
Fluoruro de estaño: fortalece el esmalte y reduce la permeabilidad.
Recomendación profesional:
«Las pastas para sensibilidad deben usarse mínimo 4 semanas para notar efecto. Evite enjuagar excesivamente después del cepillado para permitir que los activos actúen», explica el Dr. Carlos Méndez, miembro de la Asociación Dental Americana (ADA).
Tabla comparativa:
| Ingrediente | Mecanismo de acción | Tiempo de efecto |
|---|---|---|
| Nitrato de potasio | Bloqueo de terminaciones nerviosas | 2-4 semanas |
| Arginina | Sellado de túbulos dentinarios | 1-2 semanas |
| Fluoruro de estaño | Remineralización + barrera | 3-6 semanas |
5 hábitos para reducir la sensibilidad
Técnica de cepillado suave: use cepillo de cerdas ultrasuaves y ángulo de 45° hacia la encía.
Evite alimentos erosivos: refrescos, cítricos y vinagres. Enjuague con agua tras consumirlos.
Tratamiento nocturno: aplique una capa extra de pasta sensitiva con el dedo antes de dormir.
Protector bucal: si hay bruxismo, previene el desgaste.
Visite al odontólogo: descarte caries, fracturas o enfermedades gingivales.
Cuando la sensibilidad requiere atención urgente
Consulte a un especialista si:
El dolor persiste más de 30 segundos.
Hay sangrado o inflamación gingival.
Nota cambios de color en los dientes (posible pulpitis).
Dato clave: Un estudio en Journal of Clinical Periodontology (2023) vinculó la hipersensibilidad severa no tratada con un mayor riesgo de pérdida dental a largo plazo.
Soluciones profesionales
Aplicación de barnices con flúor o resinas selladoras.
Injertos gingivales en casos de recesión grave.
Láser terapéutico para cerrar túbulos dentinarios.
Prevención integral
Dieta rica en calcio y vitamina D (lácteos, espinacas, almendras).
Uso de seda dental diaria para prevenir retracciones por placa.
Control de acidez estomacal si hay reflujo.
«La sensibilidad no es normal. Si limita su vida social o alimenticia, es hora de actuar», advierte la Dra. Elena Ríos, especialista en periodoncia.
Otras noticias ...
Más allá de los dientes: 5 razones por las que tu boca es el espejo de tu futuro en 2026
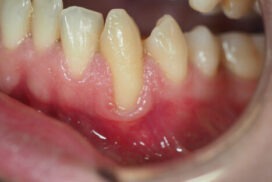
Qué puede provocar que tus encías se retraigan y qué se puede hacer para evitarlo